Перейти к:
Диабетическая ретинопатия в практике оптометриста
https://doi.org/10.33791/2222-4408-2023-3-244-251
Аннотация
Диабетическая ретинопатия – это микроангиопатия, возникающая в результате хронического длительного воздействия высокого уровня глюкозы на сетчатку глаз. В оптометрической практике специалист, с одной стороны, сталкивается с невозможностью проведения полной коррекции зрения, а с другой, может оказаться первым, кто заподозрит такую патологию и направит пациента к врачу. При этом следует отметить, что медицинские работники, специализирующиеся на лечении диабета, часто работают изолированно, что требует от пациентов посещения нескольких клиник и врачей. Несмотря на большую актуальность, во многих странах сохраняются сложности координации программ лечения узкопрофильными специалистами, которые оказывают помощь людям, живущим с сахарным диабетом. В этой статье мы обсуждаем эпидемиологию диабетической ретинопатии, описываем подход к ее оценке, диагностике и представляем обзор принципов лечения. В статье упоминается большое число лиц с диабетической ретинопатией в мире, и в том числе в России, и отмечается, что фактическая распространенность, вероятно, выше, чем сообщаемые цифры.
Ключевые слова
Для цитирования:
Сотникова Ю.П., Лоскутов И.А., Сотников Д.С., Пирятинский Б. Диабетическая ретинопатия в практике оптометриста. The EYE ГЛАЗ. 2023;25(3):244-251. https://doi.org/10.33791/2222-4408-2023-3-244-251
For citation:
Sotnikova Yu.P., Loskutov I.A., Sotnikov D.S., Piryatinsky B. Diabetic retinopathy in the practice of an optometrist. The EYE GLAZ. 2023;25(3):244-251. (In Russ.) https://doi.org/10.33791/2222-4408-2023-3-244-251
За последние три десятилетия распространенность сахарного диабета (СД) существенно увеличилась в странах с любым уровнем дохода, что отражает рост числа людей с избыточным весом или ожирением во всем мире. Глобальная распространенность диабета выросла с 4,7 % от числа населения в 1980 году до 8,5 % в 2014 году1. По данным Международной диабетической федерации, если эту тенденцию не остановить, то к 2030 году в мире будет 578 миллионов человек с сахарным диабетом, а к 2045 году – 700 миллионов.
Диабетическая ретинопатия (ДР) поражает трех из четырех человек со стажем заболевания диабетом 15 лет и более [1]. ДР была пятой по распространенности причиной предотвратимой слепоты во всем мире и пятой по распространенности причиной умеренных и тяжелых нарушений зрения у лиц в возрасте 50 лет и старше в 2020 году [2]. ДР в значительной степени связана с риском нарушения мозгового кровообращения, инфаркта миокарда и застойной сердечной недостаточности [3]. По официальной статистике на 31.12.2017 года число пациентов с ДР в Российской Федерации превысило 580 000 человек. В большинстве регионов фактическая распространенность ДР превышает регистрируемую по обращаемости в несколько раз [4]. Именно по этой причине оптометрист может оказаться первым медицинским специалистом, к кому пациент обратится за помощью. Знание патогенеза и современных подходов к выявлению и лечению ДР поможет оказать качественную медицинскую помощь по своему профилю и правильно маршрутизировать пациента для наиболее ранней постановки на учет, наблюдения и лечения.
Кто болеет диабетической ретинопатией?
Факторами риска развития ДР являются прежде всего нестабильный уровень гликемии, дислипидемия, артериальная гипертензия, а также длительность заболевания диабетом.
Как классифицируется диабетическая ретинопатия?
ДР подразделяется на непролиферативную и пролиферативно-прогрессирующую стадии.
Непролиферативная ДР (НПДР) характеризуется прогрессирующими внутриретинальными микрососудистыми изменениями (рис. 1). Прогрессирующая ДР (ПДР) характеризуется ростом новообразованных сосудов на сетчатке или диске зрительного нерва. На любой стадии ДР возможно возникновение диабетической макулопатии, в том числе диабетического макулярного отека (ДМО). ДМО сопровождается отеком и утолщением сетчатки в заднем полюсе глаза.
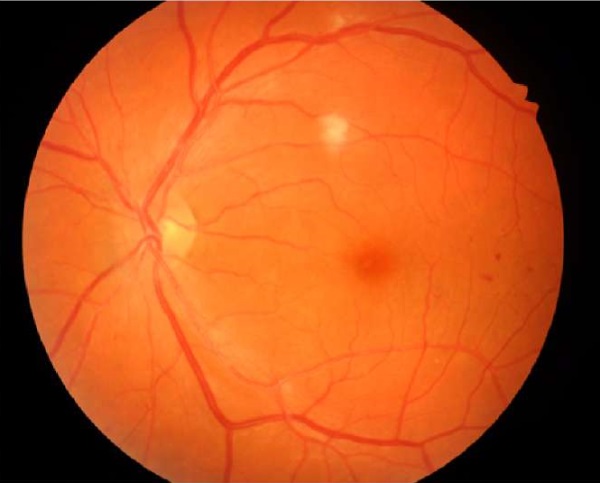
Рис. 1. Непролиферативная ангиоретинопатия,
интраретинальные микрокровоизлияния,
микроаневризмы, мягкие ватообразные экссудаты
Fig. 1. Non-proliferative angioretinopathy, intraretinal microbleeds,
microaneurysms, soft cotton-like exudates
Каковы симптомы при развитии диабетической ретинопатии?
Основной критерий – это состояние остроты зрения. НПДР обычно протекает бессимптомно. Если развивается ПДР, пациенты могут обнаружить внезапную потерю зрения из-за кровоизлияния в стекловидное тело. Более постепенную потерю зрения могут заметить пациенты, если развивается ДМО.
Как оценивается и диагностируется диабетическая ретинопатия?
Комплексное обследование глаз у человека с ДР включает измерение максимально возможной остроты зрения, внутриглазного давления, оценку переднего сегмента с помощью биомикроскопии, при необходимости гониоскопию (например, при повышенном внутриглазном давлении, глаукоме или неоваскуляризации радужной оболочки), а также исследование глазного дна на широком зрачке.
Клинический диагноз и характеристика ДР основаны на типичных аномалиях, обнаруженных при осмотре глазного дна. Ключевыми признаками НПДР являются микроаневризмы (мешковидные выпячивания стенок капилляров сетчатки из-за потери перицитов), точечные внутриретинальные кровоизлияния, наличие экссудата (рис. 2), венозное бисероплетение (сегментарное расширение вен сетчатки, которое представляет собой очаги венозной пролиферации эндотелиальных клеток), внутриретинальные микрососудистые нарушения (расширенные остатки капилляров), возникающие вторично в результате обширной облитерации капиллярных сетей между артериолами и венулами, что в итоге способствует развитию ишемических процессов в сетчатке и новообразованных сосудов. ПДР характеризуется наличием новообразованных сосудов на диске зрительного нерва, в сетчатке или в радужке. В развитой стадии ПДР пролиферация фиброзной ткани может привести к эпиретинальному фиброзу с искажением профиля макулы, кровоизлияниям в стекловидное тело (рис. 3) и тракционным отслойкам сетчатки.
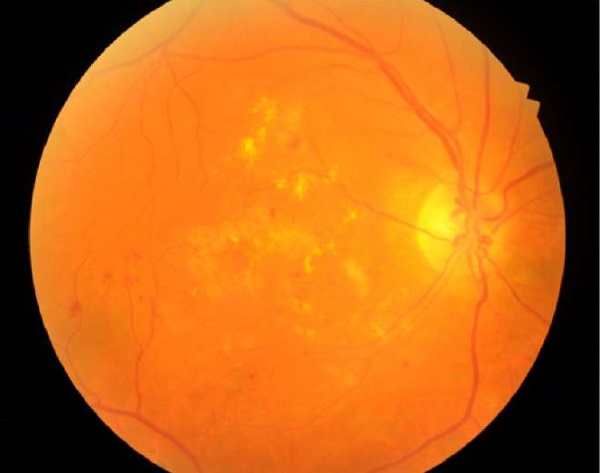
Рис. 2. Непролиферативная ангиоретинопатия,
интраретинальные микрокровоизлияния,
микроаневризмы, мягкие и твердые экссудаты
Fig. 2. Non-proliferative angioretinopathy, intraretinal microbleeds,
microaneurysms, soft and hard exudates
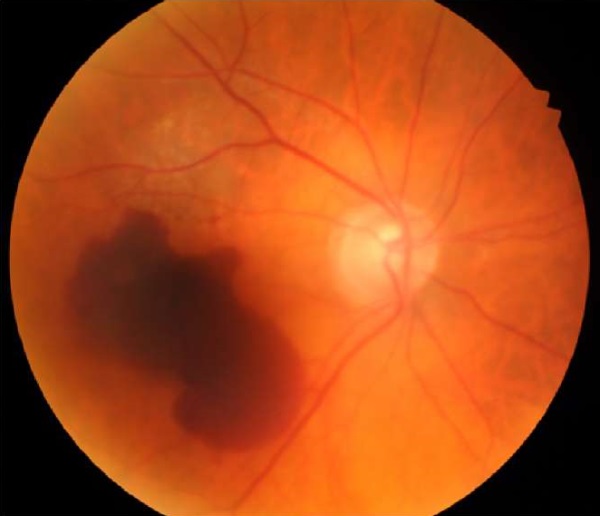
Рис. 3. Пролиферативная диабетическая ангиоретинопатия.
Преретинальное обширное кровоизлияние,
интраретинальные микрокровоизлияния,
отложения твердых экссудатов
Fig. 3. Proliferative diabetic angioretinopathy.
Preretinal extensive hemorrhage,
intraretinal microbleeds, deposits of solid exudates
Каковы принципы лечения диабетической ретинопатии?
Принципы ведения можно в общих чертах разделить на профилактику, раннее выявление и офтальмологическое лечение, направленное на снижение риска потери зрения у пациентов с осложнениями, угрожающими зрению.
Контроль гипергликемии имеет решающее значение для минимизации риска возникновения и прогрессирования ДР. Систематический обзор с метаанализом и последовательный анализ клинических испытаний показали, что строгий контроль гликемии приводит к снижению риска развития ДР на 20 % [5].
Контроль артериальной гипертензии также играет важную роль для снижения риска прогрессирования ДР. В исследовании UKPDS (United Kingdom Prospective Diabetes Study (проспективное изучение диабета в Великобритании)) пациенты с артериальной гипертензией и сахарным диабетом 2-го типа были распределены на 2 группы: интенсивного контроля артериального давления (<150/85 мм рт. ст.) и менее интенсивного контроля артериального давления (<180/105 мм рт. ст.). После 7,5 года наблюдения было отмечено снижение скорости прогрессирования ДР на 34 % в первой и ухудшение остроты зрения на три строки или более у 47 % испытуемых во второй группе [6].
Лечение дислипидемии также оказывает статистически достоверное влияние на течение ДР. Рандомизированное исследование «Действие по контролю сердечно-сосудистого риска при диабете» показало, что у людей с сахарным диабетом 2-го типа с повышенным уровнем триглицеридов, получавших симвастатин и фенофибрат, частота прогрессирования ДР через 4 года была ниже по сравнению с группой получавших плацебо [7]. Эти результаты согласуются с результатами исследования монотерапии фенофибратом, которое показало значительное снижение потребности в лазерной терапии ПДР по сравнению с группой пациентов, получавших плацебо [8].
Регулярные осмотры офтальмолога значительно снижают риск потери зрения среди людей, страдающих диабетом. Угрожающая зрению ретинопатия может не вызывать симптомов до тех пор, пока заболевание не перейдет в стадию прогрессирования и необратимой потери зрения. Лечение наиболее эффективно, если оно начато до того, как произошла серьезная потеря зрения. Эти факты подтверждают важность скрининга и эпиднадзора за ДР. Поэтому всем пациентам с СД необходимо проходить регулярные осмотры у офтальмолога не реже 1 раза в год (рис. 4). Для фотодокументации используется фотографирование глазного дна с помощью фундус-камеры. Для диагностики динамического наблюдения и контроля за лечением с целью его количественной и качественной оценки, а также мониторирования эффективности лечения ДМО применяется оптическая когерентная томография сетчатки (ОКТ, рис. 5). При диагностике заболевания, динамическом наблюдении и контроле за лечением пациентам со сниженным зрением с целью выявления и оценки площади ишемических зон в макулярной области, а также пациентам с ранней ретинальной неоваскуляризацией для ее точной локализации рекомендовано проводить оптическое исследование сетчатки с помощью компьютерного анализатора в режиме ангиографии (оптическая когерентная томография в режиме ангиографии, ОКТ-А).
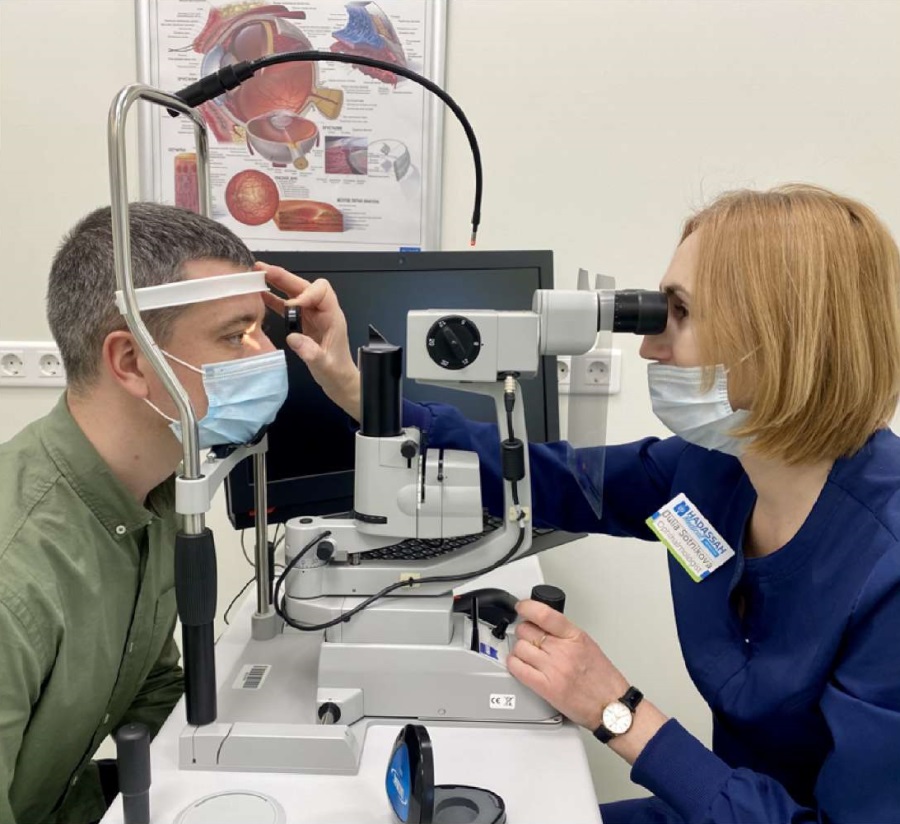
Рис. 4. Проведение биомикроскопии глазного дна
с помощью щелевой лампы и высокодиоптрийной линзы.
Обратная офтальмоскопия
Fig. 4. Conducting fundus biomicroscopy
using a slit lamp and a high-diopter lens.
Reverse ophthalmoscopy
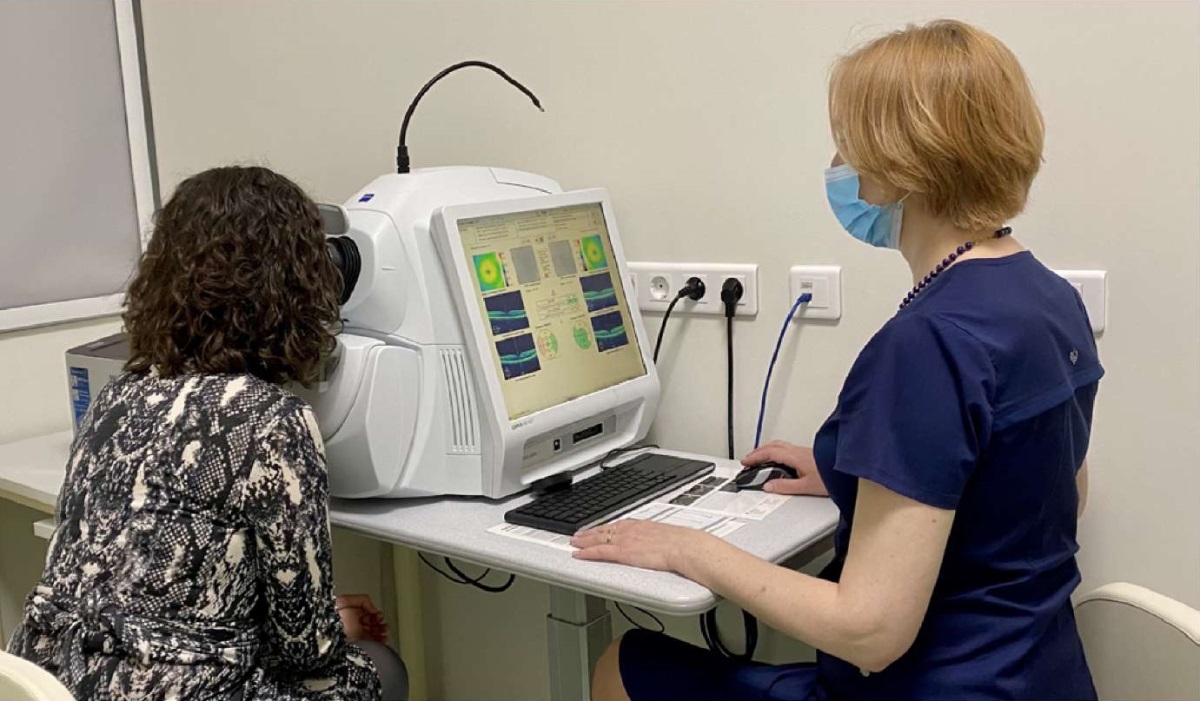
Рис. 5. Проведение оптической когерентной томографии
Fig. 5. Conducting optical coherence tomography
Офтальмологические методы лечения диабетической ретинопатии в настоящее время включают лазерную фотокоагуляцию сетчатки, которая эффективна в снижении тяжелой потери зрения, вызванной пролиферативной диабетической ретинопатией, витрэктомию, которая обычно используется при нерассасывающихся кровоизлияниях в стекловидное тело, связанных с пролиферативной диабетической ретинопатией, и интравитреальное введение фармакотерапевтических антиангиогенных и стероидных средств, что в корне изменило парадигму лечения диабетического макулярного отека и привело к значительному снижению потери зрения.
В 70-е годы прошлого века для лечения сетчатки стали применяться лазерные методы, что стало революционным поворотом в устранении ДР и помогло сохранить зрение многим пациентам, которые ранее были обречены на слепоту.
Данные клинических исследований, проведенных в 1970-х и 1980-х годах, подтвердили эффективность использования лазерной коагуляции сетчатки (ЛКС) при ПДР. Исследование диабетической ретинопатии, в котором сравнивали применение ЛКС с отсутствием ЛКС у людей с ПДР, продемонстрировало, что ЛКС снижает риск тяжелой потери зрения в результате ПДР на 50 % и более [9][10]. Согласно результатам исследования ETDRS (Early Treatment Diabetic Retinopathy Study (исследование раннего лечения диабетической ретинопатии)), не рекомендовано применять ЛКС в глазах с начальной и умеренной НПДР, но она может быть рекомендована для глаз с тяжелой НПДР. Кроме того, в исследовании ETDRS было доказано, что фокальная лазерная коагуляция клинически значимого ДМО снижает риск потери зрения на 50 % [11]. Механизмы, с помощью которых ЛКС оказывает лечебный эффект, до конца еще не изучены. Один из них заключается в том, что ишемизированная зона сетчатки разрушается с помощью ЛКС, тем самым уменьшая ангиогенный стимул. Другой возможный механизм заключается в том, что ЛКС увеличивает поступление кислорода от сосудистой оболочки к внутренней сетчатке, что становится возможным благодаря образованию лазерных рубцов из-за истончения сетчатки [12].
Витрэктомия
Витрэктомия является стандартным методом лечения нерассасывающихся кровоизлияний в стекловидное тело, связанных с ПДР, с 1970-х годов. Сегодня витрэктомия играет ведущую роль в лечении тяжелой фиброваскулярной пролиферации при ПДР [13].
Интравитреальная фармакотерапия
В настоящее время принципы лечения ДМО сместились в сторону интравитреальной фармакотерапии, включая антиангиогенную терапию (анти-VEGF) и введение стероидов. Внедрение в практику интравитреальных фармакотерапевтических средств оказало значительное влияние на уменьшение потери зрения у пациентов с ДМО. На ранних стадиях лечения ДМО часто требуются ежемесячные интравитреальные инъекции. Как только заболевание стабилизируется, интервал между инъекциями может быть увеличен, что позволяет проводить их реже с последующим динамическим наблюдением. В среднем в год требуется около 8 интравитреальных инъекций ингибиторов ангиогенеза на протяжении 1–3 лет до стабилизации процесса [14][15].
Интравитреальное введение стероида дексаметазона в виде имплантата рекомендуется пациентам с ДМО, резистентным к лечению средствами, препятствующими новообразованию сосудов, и лазерному лечению, особенно в случаях артифакии, а также пациентам с высоким кардиоваскулярным риском [16].
В последние годы активно ищутся пути, способствующие регенеративным процессам в поврежденных тканях сетчатки. В связи с этим нам представляется заслуживающим внимания применение биогенных пептидов в комплексном лечении ДР [17]. Применение пептидов на ранней стадии НПДР снижает риск прогрессирования этого осложнения. По данным доплерографии глазничной артерии [18] выявлено снижение значения индекса резистентности глазничной артерии с 0,73 ± 0,03 до 0,67 ± 0,03 (p = 0,00002) при норме 0,61–0,69 у 60 % пациентов, что показывает благоприятное воздействие пептидов на стенки капилляров бассейна глазничной артерии. Кроме того, по результатам проведенного исследования in vitro [19] было показано, что изучаемый пептидный препарат связывается с рецепторами, ассоциированными с потерей ганглионарных клеток сетчатки, а именно с глутаматными рецепторами подтипов AMPA, NMDA и mGluR1. В эксперименте in vivo получены данные биораспределения препарата при внутривенном, внутримышечном и парабульбарном режимах введения, показана динамика накопления препарата в тканях головного мозга и глаз. Взаимодействие биогенных пептидов с данными рецепторами потенциально обеспечивает нейропротекторный эффект, что способствует сохранению морфологической структуры сетчатки, стимулирует дифференцировку нейронов и клеток пигментного эпителия, стимулирует экспрессию маркеров дифференцировки клеток сетчатки и пигментного эпителия путем связывания с промоторными участками генов.
Следует отметить, что ДР в совокупности с микроальбуминурией и периферической невропатией являются гораздо лучшими предикторами сердечно-сосудистых заболеваний, чем классические факторы риска, такие как уровень холестерина и наличие гипертонии [20]. Важной концепцией является то, что ДР ассоциируется не только с нефропатией, невропатией или сердечно-сосудистыми заболеваниями, но также с деменцией [21], болезнью Альцгеймера и другими когнитивными нарушениями. Понимание этого имеет решающее значение не только для улучшения нашего видения ДР, но и для внедрения своевременного и эффективного подхода персонализированной медицины.
Первой офтальмологической проблемой, с которой сталкивается пациент при развитии ДР, является снижение зрения. И именно с жалобой на снижение зрения пациент в первую очередь обращается к оптометристу. Поэтому очень важно на этапе подбора очков заподозрить это заболевание, объяснить пациенту возможные риски и осложнения, а также рассказать о современных возможностях лечения ДР и дать соответствующие рекомендации по дальнейшему обследованию.
Вклад авторов: авторы внесли равный вклад в эту работу.
Концепция и дизайн, сбор и анализ литературы, написание статьи: Ю. П. Сотникова, Д. С. Сотников.
Критический пересмотр статьи в части значимого интеллектуального содержания, окончательное одобрение варианта статьи для опубликования: И. А. Лоскутов.
Критический пересмотр статьи в части значимого интеллектуального содержания: Б. Пирятинский.
Authors’ contributions: authors contributed equally to this work.
Design of the review, literature data collection and analysis, writing the article: Yu.P. Sotnikova, D.S. Sotnikov.
Critical revision of the article in terms of meaningful intellectual content, final approval of the version of the article for publication: I.A. Loskutov.
Critical revision of the article in terms of meaningful intellectual content: B. Piryatinsky.
1. Глобальный доклад по диабету. Женева. Всемирная организация здравоохранения. 2018;4. URL: https://apps.who.int/iris/bitstream/handle/10665/275388/9789244565254-rus.pdf (Дата обращения: 25.07.23)
Global Diabetes Report. Geneva. World Health Organization. 2018;4. URL: https://apps.who.int/iris/bitstream/handle/10665/275388/9789244565254-rus.pdf (Accessed: 25.07.23)
Список литературы
1. Fung T.H., Patel B., Wilmot E.G., Amoaku W.M. Diabetic retinopathy for the non-ophthalmologist. Clin Med (Lond). 2022;22(2):112–116. https://doi.org/10.7861/clinmed.2021-0792
2. GBD 2019 Blindness and Visual Impairment Collaborators. Causes of blindness and visual impairment in 2020 and trends over 30 years, and prevalence of avoidable blindness in relation to vision 2020: the Right to Sight: an analysis for the Global Burden of Disease Study. Lancet Glob Health. 2021;9:144–160. https://doi.org/10.1016/S2214-109X(20)30489-7
3. Modjtahedi B.S., Wu J., Luong T.Q. et al. Severity of diabetic retinopathy and the risk of future cerebrovascular disease, cardiovascular disease, and all-cause mortality. Ophthalmology. 2021;128:1169–1179. https://doi.org/10.1016/j.oph-tha.2020.12.019
4. Липатов Д.В., Викулова О.К., Железнякова А.В. и др. Эпидемиология диабетической ретинопатии в Российской Федерации по данным федерального регистра пациентов с сахарным диабетом. Сахарный диабет. 2018;21(4):230– 240. https://doi.org/10.14341/DM9797
5. UK Prospective Diabetes Study (UKPDS) Group. Intensive bloodglucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet. 1998;352:837–853.
6. UK Prospective Diabetes Study Group. Tight blood pressure control and risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 38. BMJ. 1998;317:703–713.
7. The ACCORD Study Group, ACCORD Eye Study Group. Effects of medical therapies on retinopathy progression in type 2 diabetes. N Eng J Med. 2010;363:233–244. https://doi.org/10.1056/NEJMoa1001288
8. Keech A.C., Mitchell P., Summanen P.A. et al. Effect of fenofibrate on the need for laser treatment for diabetic retinopathy (FIELD study): a randomised controlled trial. Lancet. 2007;370:1687–1697. https://doi.org/10.1016/S0140-6736(07)61607-9
9. The Diabetic Retinopathy Study Research Group. Photocoagulation treatment of proliferative diabetic retinopathy: the second report of diabetic retinopathy study findings. Ophthalmology. 1978;85:82–106.
10. The Diabetic Retinopathy Study Research Group. Photocoagulation treatment of proliferative diabetic retinopathy. Clinical application of Diabetic Retinopathy Study (DRS) findings, DRS Report Number 8. Ophthalmology. 1981;88:583–600.
11. Early Treatment Diabetic Retinopathy Study Research Group. Early photocoagulation for diabetic retinopathy. ETDRS report number 9. Ophthalmology. 1991;98:766–785.
12. Weiter J.J., Zuckerman R. The influence of the photoreceptor-RPE complex on the inner retina. An explanation for the beneficial effects of photocoagulation. Ophthalmology. 1980;87:1133–1139.
13. Machemer R., Blankenship G. Vitrectomy for proliferative diabetic retinopathy associated with vitreous haemorrhage. Ophthalmology. 1981;88:643–646.
14. Maturi R.K., Glassman A.R., Josic K. et al. Effect of intravitreous antivascular endothelial growth factor vs sham treatment for prevention of vision-threatening complications of diabetic retinopathy: The protocol W randomised clinical trial. JAMA Ophthalmol. 2021;139:701–712. https://doi.org/10.1001/jamaophthalmol.2021.0606
15. Sivaprasad S., Prevost A.T., Vasconcelos J.C. et al. Clinical efficacy of intravitreal aflibercept versus panretinal photocoagulation for best corrected visual acuity in patients with proliferative diabetic retinopathy at 52 weeks (CLARITY): a multicentre, single-blinded, randomised, controlled, phase 2b, non-inferiority trial. Lancet. 2017;389:2193–2203. https://doi.org/10.1016/S0140-6736(17)31193-5
16. Schmidt-Erfurth U. et al. Guidelines for the Management of Diabetic Macular Edema by the European Society of Retina Specialists (EURETINA). Ophthalmologica. 2017;237(4):185– 222. https://doi.org/10.1159/000458539
17. Егоров Е.А. Опыт применения Ретиналамина при различных офтальмологических заболеваниях. Клиническая офтальмология. 2017;18(1):35–38. https://doi.org/10.21689/2311-7729-2017-17-1-35-38
18. Малышева Н.А., Россохин В.Ф. Применение ретиналамина на ранней стадии лечения непролиферативной диабетической ретинопатии у детей с сахарным диабетом 1 типа. Современные технологии в медицине. 2011;3:160–161.
19. Верлов Н.А., Доротенко А.Р. и др. Исследование взаимодействия лиганд-рецептор и биораспределения лекарственного средства, содержащего полипептиды сетчатки крупного рогатого скота, при различных путях введения. Вестник офтальмологии. 2021;137(5):94–101. https://doi.org/10.17116/oftalma202113705194
20. Brownrigg J.R., Hughes C.O., Burleigh D. et al. Microvascular disease and risk of cardiovascular events among individuals with type 2 diabetes: a population-level cohort study. Lancet Diabetes Endocrinol. 2016;4(7):588–97. https://doi.org/10.1016/S2213-8587(16)30057-2
21. Simó R., Ciudin A., Simó-Servat O. et al. Cognitive impairment and dementia: a new emerging complication of type 2 diabetes-The diabetologist’s perspective. Acta Diabetol. 2017;54(5):417–424. https://doi.org/10.1007/s00592-017-0970-5
Об авторах
Ю. П. СотниковаРоссия
Сотникова Юлия Петровна, врач-офтальмолог высшей категории, ведущий специалист
121205, г. Москва, Большой бульвар, д. 46, стр. 1
И. А. Лоскутов
Россия
Лоскутов Игорь Анатольевич, доктор медицинских наук, главный офтальмолог Московской области, руководитель офтальмологической службы, заведующий научным отделом и кафедрой офтальмологии и оптометрии
129090, г. Москва, пр. Мира, д. 61/2
Д. С. Сотников
Россия
Сотников Дмитрий Сергеевич, начальник терапевтического отделения медицинского отряда
194044, г. Санкт-Петербург, ул. Академика Лебедева, д. 6ж
Б. Пирятинский
Израиль
Пирятинский Борис, кандидат медицинских наук, ведущий хирург глазного отделения
4941492, г. Петах-Тиква, ул. Жаботинского, д. 39
Рецензия
Для цитирования:
Сотникова Ю.П., Лоскутов И.А., Сотников Д.С., Пирятинский Б. Диабетическая ретинопатия в практике оптометриста. The EYE ГЛАЗ. 2023;25(3):244-251. https://doi.org/10.33791/2222-4408-2023-3-244-251
For citation:
Sotnikova Yu.P., Loskutov I.A., Sotnikov D.S., Piryatinsky B. Diabetic retinopathy in the practice of an optometrist. The EYE GLAZ. 2023;25(3):244-251. (In Russ.) https://doi.org/10.33791/2222-4408-2023-3-244-251




























